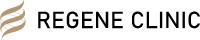間葉系幹細胞(MSC)の原理
間葉系幹細胞(MSC)とは
間葉系幹細胞(Mesenchymal Stem Cells、MSC)は、多能性を持つ幹細胞の一種で、骨、軟骨、脂肪、筋肉、神経などのさまざまな細胞に分化する能力を持っています。主に骨髄や脂肪組織、臍帯血などの間葉組織に存在し、自己複製能力や免疫調節作用も備えているため、再生医療や免疫療法の分野で注目されています。
具体的には、MSCは組織の損傷を修復するために分化して新たな細胞を供給し、また免疫系を調整することで自己免疫疾患や移植後の拒絶反応を抑えることができると期待されています。さらに、美容医療の分野でも、MSC由来の成分を利用して肌の再生やアンチエイジングケアに役立てる研究が進められています。このように、MSCはその多様な能力により、さまざまな医療や研究分野で幅広い応用が期待されています。
間葉系幹細胞(MSC)の組織修復
下記の図は、MSCの遊走と組織修復の関係の模式図です。MSCは損傷組織から放出される傷害シグナルを感知すると、末梢循環を通じて骨髄から傷害組織へと移動し、様々な化学的因子によって制御されます。損傷組織部位に到達したMSCは、パラクラインメカニズムと指向性分化という2つの重要な役割を通して、損傷組織の創傷治癒を行います。
間葉系幹細胞(MSC)の
ホーミング効果
MSCの「ホーミング効果」とは、損傷や炎症が発生している特定の組織や部位にMSCが自発的に移動する能力のことを指します。これは幹細胞が化学的シグナルに誘導されて損傷部位に向かい、修復や再生に寄与するという現象です。
MSC治療の強み
MSCベースの治療の主な利点は、損傷組織に優先的にホーミングする能力。
優先的なホーミング
損傷を受けた組織に優先的にホーミングする。
組織再生のカギ
MSCsのホーミングは組織再生において重要であると考えられており、これは幹細胞や前駆細胞が、修復を必要とする損傷組織にリクルートしてホーミングする能力を反映しています。
2種類のホーミング
炎症部位への白血球の遊走過程とは異なり、MSCsのホーミングは非全身的ホーミングと全身的ホーミングに分けられる。非全身的ホーミングとは、間葉系幹細胞を損傷部位に局所的に移植することであり、全身的ホーミングとは、損傷組織から放出されるホーミング促進因子の誘導のもと、血管内皮細胞を介して標的組織へMSCsが移動することです。
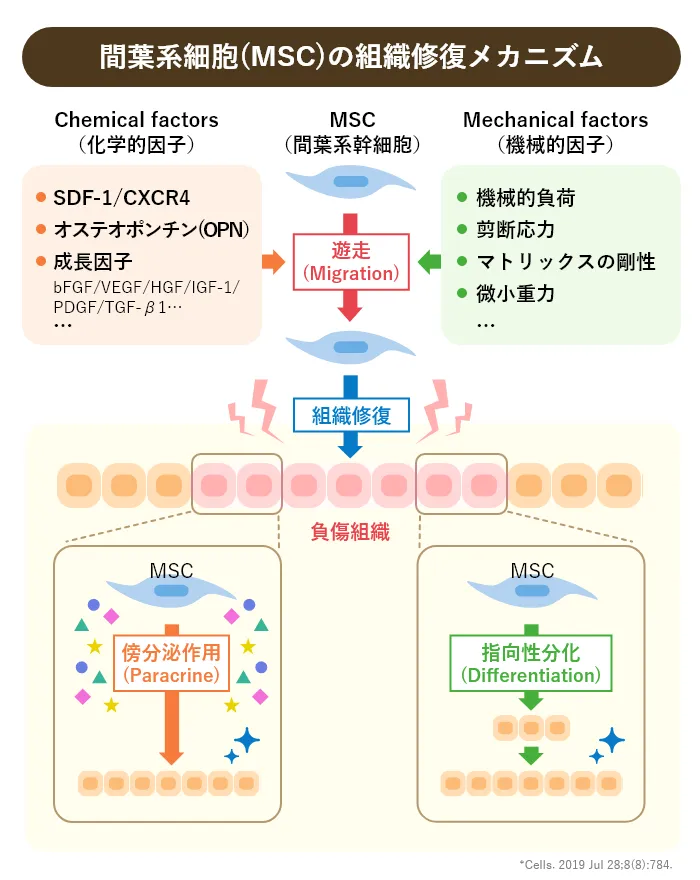
下記の図では、MSCが骨髄、筋肉、脂肪、臍帯などの組織から分離され、さまざまな種類の細胞に分化する過程や、血管内での移動(ホーミング)の過程を示しています。
※MSC(単数形)、MSCs(複数形)
間葉系幹細胞(MSC)ホーミングの
5つのステップ
1ローリング
MSCはP-セレクチン依存的に内皮細胞と結合するが、MSCはP-セレクチンリガンドを発現していないことから、他のリガンドがMSC表面のP-セレクチンと相互作用していることが示されています。骨髄MSC上に発現している糖タンパク質とガレクチン-1が、P-セレクチンの代替リガンドとして同定されている。CD44レセプターはホーミングレセプターとしても知られており、ヒアルロン酸がCD44レセプターを介したMSCsホーミングの潜在的結合部位であることが示されています。
2活性化
間質細胞由来因子-1(SDF-1)は、C-X-Cモチーフケモカインファミリーに属する小さなケモカインで、MSCsの輸送とホーミングに重要な役割を果たしています。傷害を受けた血管や組織におけるSDF-1の発現は、MSCsが発現するCXCR4へのSDF-1の結合をアップレギュレートし、MSCsがSDF-1の濃度勾配に沿って傷害を受けた組織に動員されホーミングし、その効果を発揮するように誘導します。さらに、CXCR7もSDF-1の受容体として同定され、MSCsのホーミングに関与しています。
3強固な接着
末梢血液循環に入った後、間葉系幹細胞は血管内皮細胞と絶えずローリングします。VLA4/VCAM1は、間葉系幹細胞と内皮細胞との強固な接着に重要な役割を果たしている。MSCによって発現されたVLA4は、SDF-1などのケモカインによって活性化され、内皮細胞上のVCAM1と結合して細胞接着シグナル伝達経路を活性化し、MSCと内皮細胞との接着を促進します。
4クローリング
CCR2/FROUNT/PI3Kシグナル伝達経路は、アクチンフィラメントと偽足趾の形成を促進し、それによって細胞骨格の再編成を媒介し、MSCsが血管内壁を這い回り移動するのを促進します。
5経内皮移動
MSCは、マトリックスメタロプロテアーゼ(MMP9、MT1-MMPなど)やタンパク質分解酵素(uPAなど)を分泌し、内皮基底膜とペリサイト鞘のバリアを破壊して、経上皮移動を完了します。MSCsのホーミング効率を向上させることは、MSCs治療における課題の一つです。現在、標的薬物送達、幹細胞の遺伝子工学、磁気誘導などの技術があり、様々な技術によりMSCsの組織的または非組織的ホーミング能の改善を目指しています。
間葉系幹細胞(MSC)の
免疫調整メカニズム
リンパ球および骨髄球に対するMSCの免疫調節メカニズムについて、研究で明らかになっている事象は、具体的に以下のようなことが挙げられます。
免疫の指揮官
MSCの免疫機能は、免疫応答全体を組織化する上で重要な白血球集団であるCD4 Tリンパ球に対して最もよく報告されています。
炎症から修復へ
MSCは、主にパラクリン因子、中でも形質転換成長因子β(TGF-β)、肝細胞成長因子(HGF)、プロスタグランジンE2(PGE2)、一酸化窒素(NO)、インドールアミン2,3-ジオキシゲナーゼ(IDO)を介して、エフェクターT細胞で主に満たされた炎症性環境から、制御性T(Treg)リッチな微小環境へと、これらの適応細胞を調節することが示されています。
NK細胞との協調
MSC-T細胞の免疫調節に細胞間接触が関与していることを発見した研究はいくつかありますが、このメカニズムはMSC-NK相互作用においてより顕著であり、MSCが発現する表面や、胎児-母体の免疫調節に重要な非クラシカルMHCクラスI分子である可溶性HLA-Gを介して、KIR、NKp30、NKp44、NKG2Dなどの活性化NKレセプターのダウンレギュレーションが関与しています。
広範な免疫調節
IFN-γやIL-1βを含む炎症シグナルによって誘導されるPGE2やIDOのような免疫調節性のパラクリン因子は、T細胞、NK、IL-10を発現する制御性B細胞が増殖しているB細胞を含むすべてのリンパ球を含む白血球亜集団にわたるMSCの相互作用において顕著です。
B細胞のブレーキ
MSC-B細胞相互作用に関する報告は少ないが、そのほとんどがB細胞の増殖、分化、抗体産生の抑制を示しています。
下記の図は、間葉系幹細胞(MSC)がリンパ系細胞や骨髄系細胞にどのように作用するかを示しています。
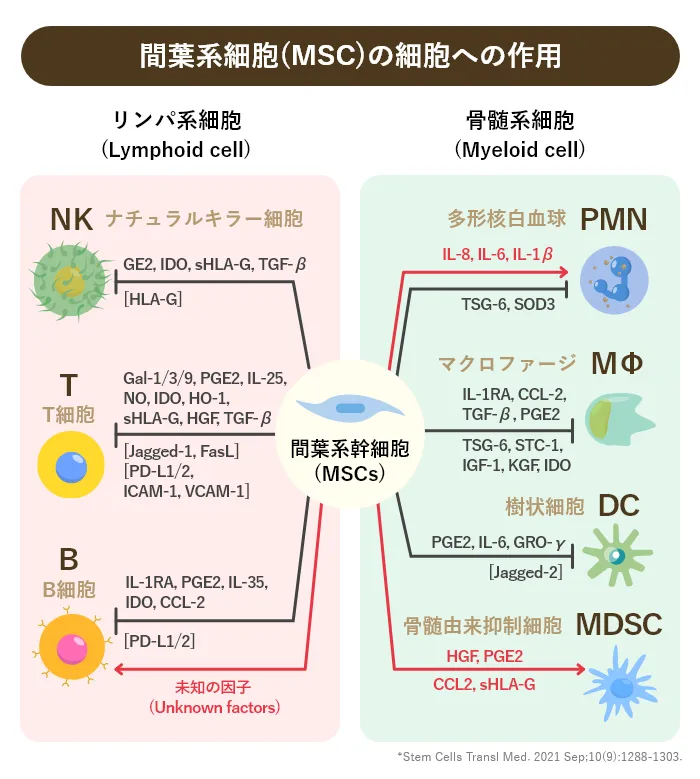
免疫反応における間葉系幹細胞(MSC)の役割
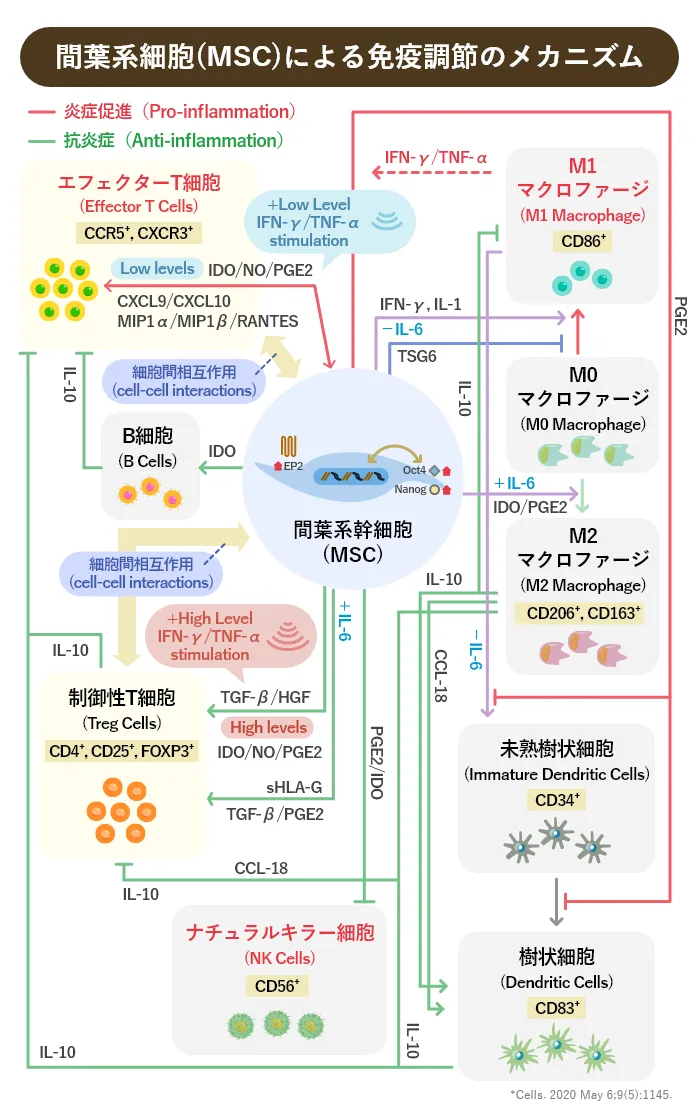
下記の図は、免疫細胞における炎症性・抗炎症性条件下でのMSCの反応と相互作用を分類した図です。これらの作用は、細胞間接触を介したB細胞およびT細胞の増殖抑制、制御性T細胞の誘導およびトランスフォーミング増殖因子(TGF-)/肝細胞増殖因子(HGF)を介した制御を示しています。また、ナチュラルキラー(NK)細胞、様々な成熟段階にある樹状細胞(DC)、および微小環境に依存するマクロファージ分極を抑制することにより、MSCの免疫調節能力を示しています。
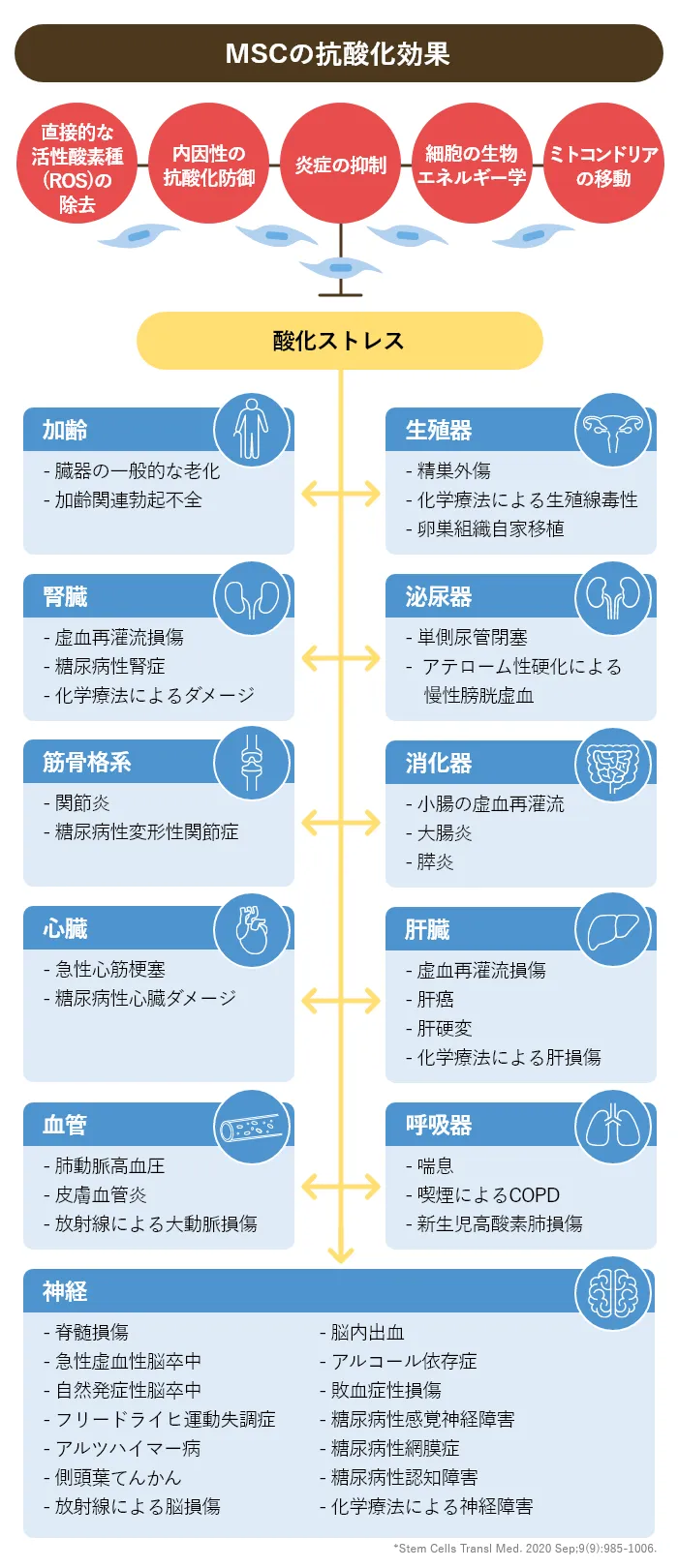
間葉系幹細胞(MSC)の抗酸化作用
MSCは、フリーラジカルの消去やミトコンドリアの提供によって直接的に、あるいは他の細胞における抗酸化防御のアップレギュレーションや細胞の生体エネルギーを変化させることによって間接的に、抗酸化作用を示しています。MSCの免疫抑制特性は、活性酸素種(ROS)の発生を回避することもでき、これらのメカニズムにより酸化ストレスが軽減され、様々な病態におけるMSCsの治療効果が期待されています。